引言
目前,临床中应用广泛的金属材料主要有不锈钢、钴基合金、钛及钛合金三大类[1],其中钛及钛合金材料由于具有耐腐蚀和机械加工性能良好、密度小(和人骨近似)、强度高、弹性模量低等优点,被认为是一种理想的外科植入物材料[2]。但金属钛的弹性模量约为110GPa,仍远远高于骨组织弹性模量10~30GPa,植入人体后出现应力遮挡现象的概率大,会出现各种不良反应,且金属钛的耐磨损性能较差,金属离子的溶出也是金属材料的一种通病,会引起人体的各种炎症反应。这些都是在临床上导致外科植入手术失败的重要原因[3-5]。因此,对外科植人物产品进行表面改性处理显得尤为重要,亦要对表面改性完成后的外科植入物产品进行表面形貌及表面元素分析。
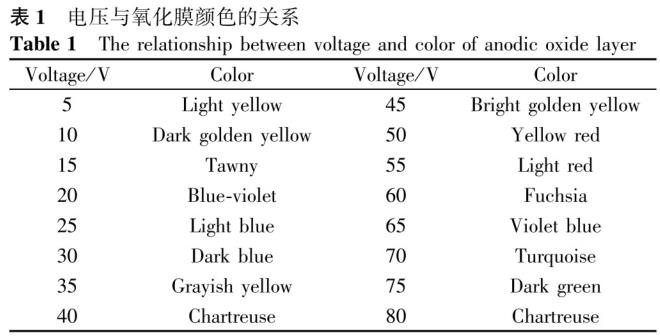
为了解决这一系列问题,对金属钛及钛合金表面进行改性处理,不仅可以将材料由“生物惰性”转变为“生物相容性”,还能够影响细胞的生物学活性和组织反应性,进而获得更好的植入物一骨组织界面结合能力[6-7]。近年来常用的表面改性手段有表面阳极氧化、等离子喷涂、喷砂酸蚀等,其中表面阳极氧化作为表面改性的重要方法之一被广泛应用于外科植人物产品中,根据工艺的不同,阳极氧化又分为着色阳极氧化(I型)和微弧阳极氧化(Ⅱ型)两种[8-10]。而阳极氧化膜的颜色变化与所加电压有密切关系[11-13](见表1),其厚度随着氧化电压的升高而增加,而不同厚度的氧化膜表面发生了光的薄膜干涉,从而呈现冉不同的颜色[14-16]。氧化膜的不同颜色也可作为区别植入物的一种方法,可以有效降低手术过程中的差错率。阳极氧化膜的实质是一层致密的氧化钛陶瓷膜,其最大的特点是:陶瓷膜在基体表面原位形成,与基体的结合非常牢固,明显提高了材料的耐磨、耐腐蚀性能,同时提高了材料的循环疲劳性能[17]。阳极氧化膜也在很大程度上解决了金属离子溶出问题,降低了细胞毒性,大大提高了植人物的生物相容性[18]。
虽然阳极氧化工艺具有很多其他表面改性工艺不具备的优点,但是在阳极氧化过程中可能会引入与基体元素不一致的其他元素[10],其中包括有意添加的Si、Ca、P等元素[19-22],及工艺引入的Na、Mg、Al、S、Fe等其他元素,因而对经过阳极氧化后的外科植入物产品表面元素的分析显得尤为重要。目前主要采用扫描电镜及能谱仪(SEM&EDS)、X射线荧光能谱仪(EDXRF)等对阳极氧化产品表面元素进行分析。对比两种方法可知,EDXRF无法检测原子序数低于Na的元素,且对Na、Mg等原子序数较低的元素区分较为困难,当元素含量较低时更甚,但此方法对样品的预处理较为简单或基本不需要预处理且实验周期较短,也是一种较为理想的分析方法。相较而言,SEM&EDS则可以有效区分原子序数在碳(C)以上(包含C元素)的元素,但对样品的预处理较为复杂,两种方法各有优劣势。
本工作通过扫描电镜及能谱仪对外科植入物阳极氧化产品表面元素进行分析并观察其表面形貌,对表面元索含量进行统计分析,为企业优化生产工艺、表面元素定量分析和生物安全性评价提供参考。
1、实验
1.1试样预处理
选取不同企业提供的外科植入物阳极氧化产品作为研究试样,采用精密切割机(Buehler,型号:HS112700)将外观尺寸比较大的试样切割成合适大小的典型性试样块,而外观尺寸合适的不需要进行切割处理,做好试样标识。然后将处理好的试样块在乙醚或丙酮等溶剂中进行浸泡清洗,在通风橱中自然干燥后将其放人干燥器中保存待用,避免其他污染。
1.2表面形貌表征
将制备好的试样用石墨导电胶粘贴在铝制样品台上,被检测面向上,将其放人扫描电镜样品室。选择合适的激发电压及电流,采用扫描电镜(Hitachi,型号:S-4800或Thermo Fisher Scientific,型号:Scios 2)对试样表面阳极氧化膜进行形貌观察和分析,同时测量微弧阳极氧化膜表面的孔径尺寸。
1.3表面元素分析
采用扫描电镜配带的能谱仪(Bruker,型号:XFlash detector 630M)在合适的激发电压下对试样表面元素含量进行分析,并对各元素分布情况进行统计分析。
2、结果与讨论
2.1阳极氧化膜成因及表面形貌分析
着色阳极氧化是在电解液中利用电极反应和电场驱动使金属离子和氧离子扩散,在阳极表面(钛及钛合金产品)形成一层致密的氧化膜,在电极两端施加不同的电压产生的氧化膜厚度不同,从而产生不同的色彩,因此,着色阳极氧化也可称为彩色阳极氧化。随着工作电压的增加颜色由黄一>蓝一>黄一>红一>紫一>绿依次发生变化。当工作电压达到一定程度时,在金属材料表面产生火花放电,继而相互融合形成放电弧斑,最终形成特异性氧化膜,这一过程被称为微弧阳极氧化[6],而颜色亦变为黑灰色.因此,微弧阳极氧化也可称为黑灰色阳极氧化。合理控制工作电压不仅表面颜色会出现不同,而且表面形貌差异较大.尤其是着色阳极氧化与微弧阳极氧化之间。
阳极氧化膜表面因T艺不同而呈现出不同形貌,如图1所示,微弧阳极氧化(见图1a)表面形貌出现多孔结构,且为均匀分布的火山口状突起。由图1b可以看出,火山口状突起内部出现很多孔洞。直径为100~300nm且出现交联,在整体上呈现立体孔隙结构。着色阳极氧化(见图lc、d)表面形貌呈不规则的凹凸不平状且均匀分布在氧化膜表面,由图lc、d内放大插图可以更清晰直观地观察到其表面不规则的凹凸不平状氧化膜。阳极氧化膜有利于提高基体的耐磨、耐腐蚀性能,还可以屏蔽金属离子溶出,对细胞生长无毒性作用。氧化膜表面的多孔结构及凹凸不平状结构均有利于细胞黏附生长,将其植入骨内有利于骨组织生长[6,14]。

2.2着色阳极氧化表面元素分布统计分析
通过对244批外科植入物着色阳极氧化产品表面元素进行分析,发现所有外科植入物氧化膜均含有O、Ti元素(基体)。表2为着色阳极氧化表面所含元素统计,可以发现着色阳极氧化膜中有11.07%的产品包含Na、Si、P、S、A1等其他元素中一种或多种,且所含各元素占比均在10%以下(其中P元素最高为8.20%,其余Na、Si、S、Al元素均小于3%)。着色阳极氧化表面出现Na、Si、P、S等元素的原因是电解液中存在上述元素,而Al元素则是电解池或清洗池采用镁铝合金材料制成或纯钛和钛合金材料共用一个清洗池引人的。
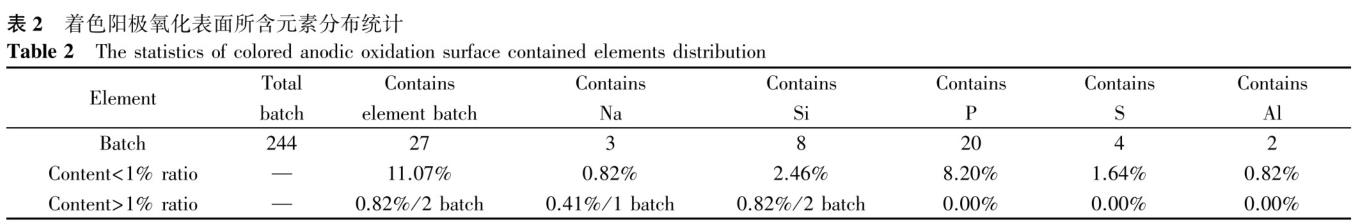
根据扫描电镜及能谱仪分析结果,将表面元素含量(质量分数)分为两个区间,分别为小于1.00%、大于1.00%,其中所含元素质量分数大于1.00%的只有2批,其余批次均小于1.00%。着色阳极氧化膜中含有的元素一般不存在有意添加的元素,都是工艺引入的杂质元素,其元素种类和含量差异较大,说明不同企业、不同生产工艺对阳极氧化膜表面所含元素的种类和含量具有很大的影响。选取着色阳极氧化表面所含Na、Si、P、S元素各2批产品进行再次清洗,将清洗后的产品重新进行检测,结果表明均未出现上述所含元素,去除率达到100%;选取所含Al元素的2批产品进行更换清洗池且纯钛和钛合金材料产品分开进行重新清洗,将清洗后的产品重新进行检测,结果表明均未出现Al元素,去除率也达到100%。综上所述,着色阳极氧化产品表面元素都是清洗不彻底、清洗池更换不及时或不同基体材料未分开进行清洗等所致,生产企业及其他科研、监管机构应予以关注。
2.3微弧阳极氧化表面元素含量分析
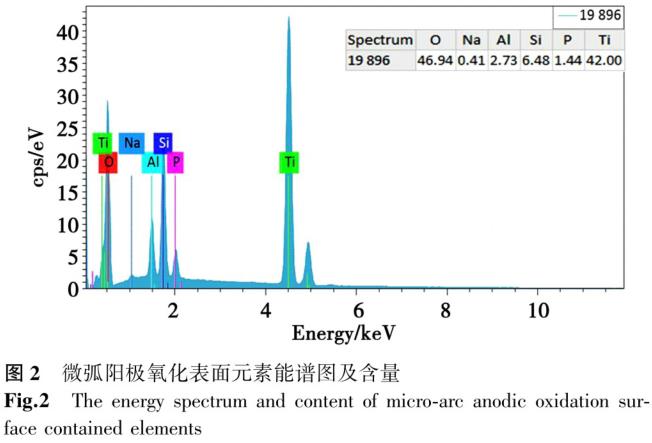
通过扫描电镜及能谱仪对微弧阳极氧化(任意选取一个试样)进行表面元素含量及面扫描分析,如图2、图3所示。图2为微弧氧化产品表面元素的能谱图及含量,基体材料为TC4。由图2可知,除基体材料元素外,表面所包含的元素为Na、Si、P。图3a为元素的总体面分布,右侧分别为表面所包含元素(Na、Si、P)及基体包含元素(Ti、A1)单一元素的分布。由图2可见,阳极氧化膜表面所包含元素均匀分布在氧化膜表面,也从侧面佐证了阳极氧化丁艺的稳定性与均匀性。

2.4微弧阳极氧化表面元素分布统计分析
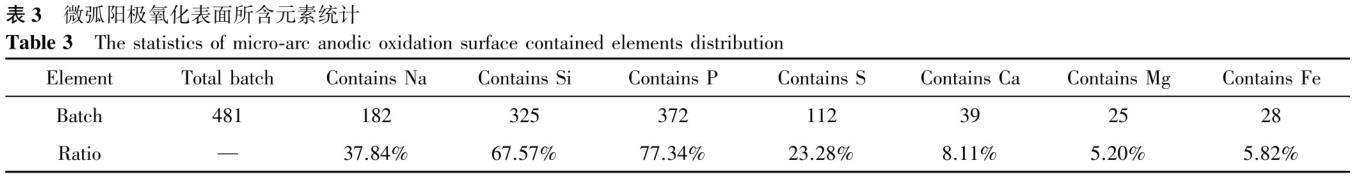
通过对481批外科植入物微弧阳极氧化产品表面元素分析可知,所有外科植入物氧化膜均含有O、Ti元素。由表3可以看出微弧氧化膜表面含有的元素种类各不相同,其中含有Si、P元素的批次较多,占总批次的65%以上,而含有Ca、Mg、Fe元素的占比相对较少,均低于10%。微弧阳极氧化表面出现Na、Si、P、S、Ca等元素的原因是电解液巾存在上述元素或有意添加的元素;Mg元素是电解池或清洗池采用镁铝合金材料制成所致;Fe元素则是阳极氧化过程中所使用工装夹具的连接用螺栓为不锈钢材质所致。
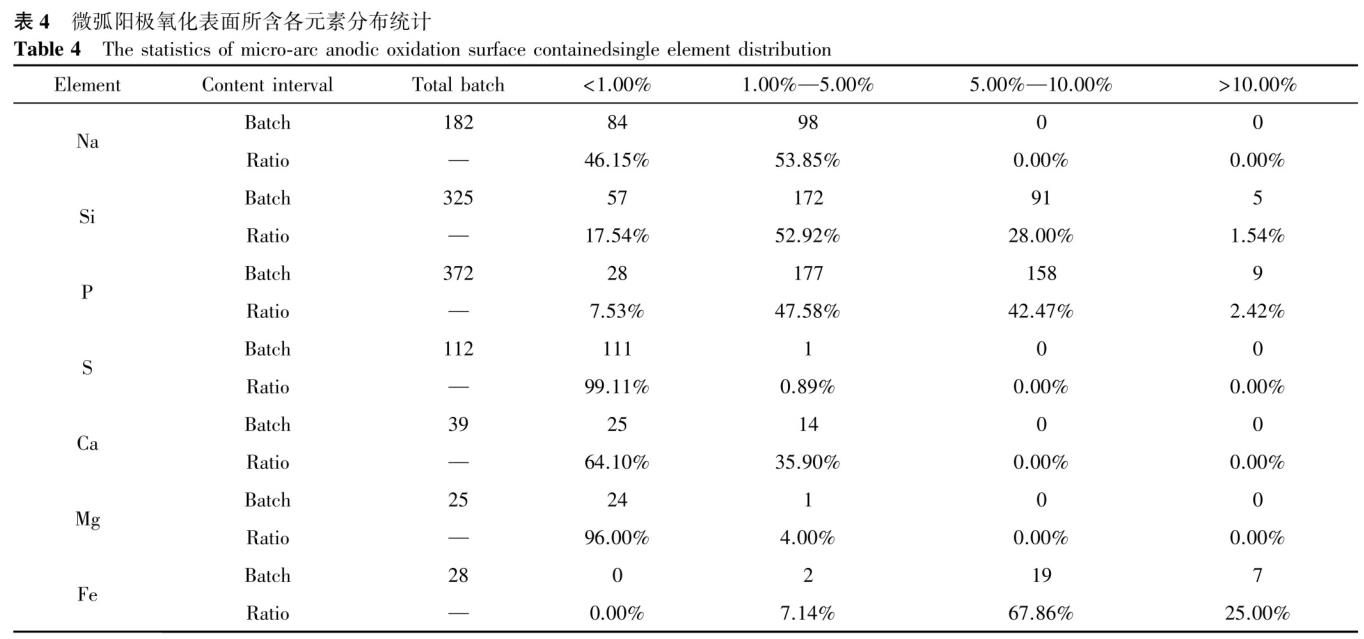
根据扫描电镜及能谱仪分析结果,对微弧氧化表面所含元素种类及含量(质量分数)分布进行统计分析,将表面所含元素含量分为四个区间,分别为小于1.00%、1.00%~5.00%、5.00%~10.00%、大于10.00%。表4为微弧氧化膜中所含Na、Si、P、S、Ca、Mg、Fe含量的分布统计。从表4中可以看出,所含Na、S、Ca、Mg含量均未出现大于5.00%的批次,且除Na元素外含量小于1.00%的批次占比均高于60%,甚至S和Mg含量小于1.00%的批次占比达到90%以上。表4巾Fe元素则未出现小于1.00%的批次,而在5.00%~10.00%区问的表4微弧阳极氧化表面所龠各元素分布统计批次占比最高达到67.86%。表4中所含Si、P元素显示四个含量区间中都有不同数量的批次进行对应,其中含量落在1.00%~10.00%IX_问的批次占比均高于80%,而含量大于10.00%的批次占比均低于3%。
综合表4来看,所有以上元素含量(质量分数)基本落在小于10.00%这个区间,但含量大于10.00%的只有Si、P、Fe元素,批次为21批,只占总批次的4.37%。总体来看,微弧氧化膜巾所含Na、Si、P、S、Ca、Mg、Fe等元素含量的分布各不相同且无统计学意义(P>0.05),再次说明不同企业、不同生产工艺对阳极氧化膜表面所含元素的种类和含量具有很大的影响,因此,企业及其他科研、监管机构应严格控制电解池及有意加入的元素限量以达到预期的效果。
3、结论
不同企业、不同生产工艺的阳极氧化膜表面所含元素的种类和含量差异较大,无法做到统一,但对优化改进企业阳极氧化工艺具有指导性意义。首先,企业应严格控制电解液的配方,且定期更换;其次,电解池和清洗池的材料选择应与植人物产品基体材料相同,避免由电解池等材料引入杂质元素(如Mg、Al等),也应避免选用与产品基体材料不同的工装夹具及连接螺栓,从而引入其他杂质元素(如Fe等元素):再次,不同材料(如纯钛和钛合金材料等)的产品应分开进行清洗,并做到充分清洗,以避免钛合金材料中的Al、V等元素引入到纯钛材料的阳极氧化表面。
对于微弧阳极氧化产品,可以添加一定比例的Ca、P元素,在植入物表面诱导产生羟基磷灰石,促进骨一植人物表面骨的形成;或添加一定量的Si元素,有利于成骨细胞的黏附、生长和增殖。对于有意添加的元素,其含量尽量落在同一区间内,以确保作用最大化;而对于工艺引入的杂质元素,其含量应尽可能低,以降低不良反应发生的可能性。此结果对后期的表面元素定量分析、生物安全性评价及临床应用均具有一定的参考价值。
参考文献
1 戴正宏.医用钛合金表面阳极氧化研究.硕士学位论文,天津大学,2004
2 黄伯云,李成功,石力开,等.有色金属材料手册,化学工业出版社.2009.PP.735.
3 Long M,Raek H J.Biomaterials,1998,19.1621.
4 Ba,rere F,vall de,Valk C M,Meijer G,et a1.Journal ofBiomedical Ma—terials Research,2003,67,655.
5 Huiskes R,Weinans H,van Rietbergen B.Clinical Orthopaedics and Re—lated Research.1992,274.124.
6 刘帅.钛合金材料表面阳极氧化和微弧氧化改性涂层的构建及生物学研究.博士学位沦文.第四军医大学.2014.
7 Buser D,Schenk R K,Steinemann S,et a1.Joumal o,Biomedical_Mate—rials Researeh,1991,25,889.
8 万智来,李玉海,蒋围瑜,等.捌料帚报,2010,24(Z2),193.
9 李维兴.科技创薪与应用。2012(18),101.
10 张晨,宋铎,樊铂,等.生物骨科材料与临床研究,2014,11(6)76.
11 周泽,曾鹏,谢光荣,等.广州化工,2006,34(6),24.
12 赵晴,杜楠,王元正,等.南昌航空工业学院学报,2000,14(1)47.
13 闫召民,郭天文,余建军,等.实用口腔医学杂志,2001,36(6)530.
14 安俊波,樊铂,宋铎,等.巾周医疗器械信息,2017(7),40.
15 师秀萍,朱永明,屠振密,等.也镀与环保,2009,29(2),25.
16 杨绿.钛及钛合金阳极氧化着色]_艺及其电源的研究.硕士学位沦文,贵州大学,2005.
17 刘亮,郭锋,李鹏飞,等.表面技术,2009,38(3),37.
18 虞崇庆,工龙浩,马骏,等.生物骨科材料与临床研究,2020,17(6),75.
19 谭思民,千帅旱,赵晴,等.表面技术,2014,3(43),20.
20 郝建民,夏慧慧,陈宏,等.材料熟处理学报,2014,35(3),184.
21 邱小忠,王永魁,王乐禹,等.中国筛床解剖学杂志,2012,30(1),84.
22 左林,柏树令,潘锋,等.解剖学杂志,2011.34(2),152.
相关链接














